
Das Infotainment-Portal für Deutschland.

Das Infotainment-Portal für Deutschland.
21 Dez 2020
London(ots) - LumiraDx, das Unternehmen der nächsten Generation in der Point-of-Care-Diagnostik, hat heute bekanntgegeben, dass es nach einer durch die Swiss Society for Microbiology (SSM) durchgeführten positiven technischen Validierung eine Autorisierung des Schweizerischen Bundesamtes für Gesundheit (BAG) für seinen LumiraDx SARS-CoV-2 Antigen Test erhalten hat. Der Schnelltest zeigte eine 98,4%-100%ige positive Übereinstimmung und 99%ige negative Übereinstimmung im Vergleich mit der RT-PCR.
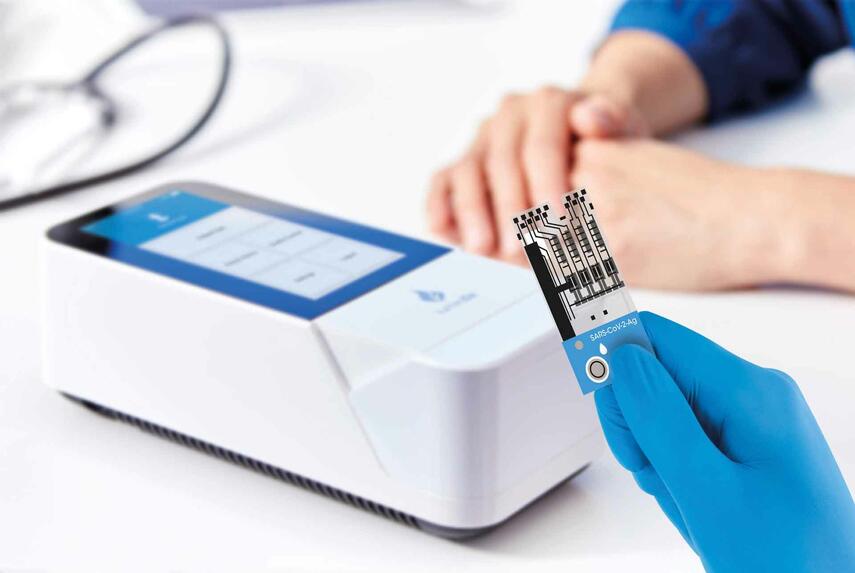
Der SARS-CoV-2 Antigen Test wird auf der LumiraDx Platform angewendet und weist das Antigen-Nukleokapsidprotein aus Nasal- und Nasopharyngealabstrichproben mit genauen qualitativen Ergebnissen in 12 Minuten nach. Er verwendet die neueste mikrofluidische Immunfluoreszenztest-Technologie, die für eine hohe Sensitivität sorgt.
"LumiraDx freut sich über die erfolgte regulatorische und vergütungstechnische Anerkennung in der Schweiz" sagt LumiraDx Chief Commercial Officer David Walton. "Wir arbeiten mit Laboratorien, Arztpraxen, Apotheken, Kliniken und Testzentren, um die medizinischen Fachkräfte mit unserer Point-of-Care-Lösung für eine hoch-sensitive COVID-19-Antigentestung in Minuten versorgen zu können."
Die technische Validierung des BAG wurde von einem beauftragten Labor unter Leitung der SSM mit einer Studie mit 100 positiven und 200 negativen Proben durchgeführt. Verglichen wurde die technische Performance des LumiraDx SARS-CoV-2 Antigen Tests mit einer Lateral-Flow-Antigen-Referenzmethode sowie mit einem PCR-System, dem Roche Cobas 6800. Die technischen Sensitivitätsdaten bei spezifischen Ct-Werten (Indikatoren für die Viruslast, bei denen ein hoher Ct-Wert einer niedrigeren Viruslast entspricht) von Ct 23, Ct 26 und Ct 29 wurden bewertet. Bei Ct 29 (niedrigste Viruslast) erreichte der LumiraDx SARS-CoV-2 Antigen Test eine positive Übereinstimmung mit der PCR von 98,7% und dagegen der Lateral-Flow-Antigentest (POCT-Referenzmethode) eine positive Übereinstimmung mit der PCR von 92%, was auf eine signifikant höhere Sensitivität des LumiraDx-Tests im Vergleich zur Lateral-Flow-Antigen-Referenzmethode hinweist. Zudem erreichte der LumiraDx SARS-CoV-2 Antigen Test eine Spezifität von 99%.
"Ein Hauptziel der COVID-19-Testprogramme ist die schnelle und zuverlässige Identifizierung infektiöser Personen. Signifikante Evidenz deutet derzeit darauf hin, dass Antigen-Testergebnisse eine bessere Indikation auf Infektiosität sein könnten als RT-PCR-Testergebnisse (molekulare Testergebnisse) und dass Personen mit hohen Ct-Werten (niedrige Viruslast) wahrscheinlich nicht infektiös sind ", sagt LumiraDx, Chief Innovation Officer Nigel Lindner. "Die technischen Validierungsergebnisse der SSM stimmen gut mit einer kürzlich erschienenen Publikation überein, in der der LumiraDx SARS-CoV-2 Antigen Test eine 100%ige positive Übereinstimmung im Vergleich zur PCR in frischen klinischen Proben mit Ct-Werten von unter 33 bei symptomatischen Probanden innerhalb von 12 Tagen nach Auftreten der Symptome zeigte. Hochsensitive Antigentests am Point of Care ermöglichen die schnelle und genaue Identifizierung infektiöser Patienten."
Über LumiraDx
LumiraDx wurde 2014 von einer Unternehmergruppe gegründet, Ron Zwanziger (Chairman und Chief Executive Officer), Dave Scott, Ph.D. (Chief Technology Officer) und Jerry McAleer, Ph.D. (Chief Scientist). Gemeinsam blicken sie auf über drei Jahrzehnte erfolgreicher Arbeit beim Aufbau und Wachstum von Diagnostikunternehmen zurück, darunter bei Unternehmen wie Medisense Inc., Inverness Medical Technology Inc. und Alere Inc. Das Unternehmen wird von institutionellen und strategischen Investoren wie unter anderem der Bill & Melinda Gates Foundation, Morningside Ventures und U.S. Boston Capital Corporation unterstützt. Der Firmenhauptsitz von LumiraDx ist in Großbritannien und Konzerngesellschaften auf der ganzen Welt mit Zugang zu allen wichtigen Märkten unterstützen den Vertrieb. Weltweit beschäftigt LumiraDx mehr als 1000 Mitarbeiter.
LumiraDx befasst sich mit Entwicklung, Produktion und Vertrieb einer innovativen diagnostischen Platform für den Point-of-Care-Einsatz. Die LumiraDx Platform wurde entwickelt, um in Minutenschnelle mit Labormethoden vergleichbare diagnostische Ergebnisse am Point-of-Care zu liefern. Sie ist als kostengünstige und leicht zugängliche Lösung für medizinische Einrichtungen auf der ganzen Welt konzipiert, wobei speziell die dezentrale Versorgung im Fokus steht.
Quelle-Bild: obs/LumiraDx